Artículo de Revisión
Infección por Helicobacter pylori, una revisión actualizada
María Nordmann-Ricardo, Yiser Martínez1, Daniela García1, Odalys Cardona1, Andrés Sánchez2, Marlon Múnera
ARCHIVOS DE ALERGIA E INMUNOLOGÍA CLÍNICA 2021;( 04):0142-0148 | DOI: 10.53108/AAIC/202104/0142-0148
Antecedentes. Helicobacter pylori es una bacteria Gram negativa, microaerofílica en forma de espiral, posee distintos factores de virulencia los cuales le permiten desarrollar la enfermedad e inducen mayor incidencia y prevalencia de su patogenicidad como: la ureasa, flagelo, gen cagA, citoxina vacA y proteína babA. Tiene una amplia capacidad para sobrevivir o adaptarse a condiciones extremadamente ácidas del entorno gástrico. Ocasiona dispepsia, sensación de hinchazón del estómago, náuseas, vómitos, entre otros. Su prevalencia está relacionada con un bajo índice socioeconómico y malas condiciones higiénicas. Además, es considerado la principal causa de gastritis crónica, el principal agente etiológico de cáncer gástrico y la enfermedad ulceropéptica, y por último también se ha relacionado con el linfoma del tejido linfoide asociado a las mucosas (MALT, por sus siglas en inglés: mucosa-associated lymphoid tissue).
Objetivo. Generar una actualización del estado del arte sobre H. pylori.
Conclusiones. H. pylori sigue siendo considerado un patógeno de alta relevancia para el desarrollo de gastritis, y su papel en el desarrollo de cáncer gástrico se mantiene de interés dado su difícil control.
Palabras clave: Helicobacter pylori, neoplasias gástricas, dispepsia, inhibidores de la bomba de protones.
Background. Helicobacter pylori is a Gram negative bacterium, microaerophilic in the form of a spiral, it has different virulence factors which allow it to develop the disease and induce a higher incidence and prevalence of its pathogenesis such as: urease, flagellum, cagA gene, cytoxina vacA and protein slime. It has a broad ability to survive or adapt to extremely acidic conditions in the gastric environment. It causes dyspepsia, a feeling of bloating in the stomach, nausea, vomiting, among others. Its prevalence is related to a low socioeconomic index and poor hygienic conditions. In addition, it is considered the main cause of chronic gastritis, the main etiological agent of gastric cancer and peptic ulcer disease and finally it has also been related to mucosa-associated lymphoid tissue lymphoma (MALT, for its acronym: mucosa-associated lymphoid tissue).
Objective: Generate an update on the state of the art on H. pylori.
Conclusions: H. pylori is still considered a highly relevant pathogen for the development of gastritis, and its role in the development of gastric cancer remains of interest given its difficult control.
Keywords: Helicobacter pylori, gastric neoplasms, dyspepsia, proton pump inhibitors.
Los autores declaran no poseer conflictos de intereses.
Fuente de información Asociación Argentina de Alergia e Inmunología Clínica. Para solicitudes de reimpresión a Archivos de Alergia e Inmunología Clínica hacer click aquí.
Recibido 2021-09-23 | Aceptado 2021-11-08 | Publicado 2021-12-30
Introducción
Helicobacter pylori es una bacteria Gram negativa, microaerofílica en forma de espiral, la cual posee de cinco a seis flagelos que le permiten su movilización y adherencia al epitelio gástrico1. Esta bacteria está asociada a la gastritis y a la enfermedad ulcerosa peptídica, además se la considera factor de riesgo en el cáncer gástrico.
Patogenicidad
Debemos tener en cuenta que H. pylori posee distintos factores de virulencia los cuales le permiten desarrollar la enfermedad e inducen mayor incidencia y prevalencia de su patogenicidad. Los factores de virulencia más importantes que esta tiene son: la ureasa, el flagelo, el gen cagA, la citotoxina vacA y la proteína babA
En primera instancia la ureasa es la enzima más abundante que produce H. pylori, la actividad de esta depende del pH en el que se encuentre la bacteria, se debe tener en cuenta que el hábitat natural de H. pylori se encuentra por debajo de la capa mucosa, donde el pH se aproxima a la neutralidad, es por esto que el mecanismo que utiliza para protegerse de ese pH ácido durante la colonización se basa en acumular una gran cantidad de ureasa en el citoplasma, en el espacio periplásmico y en la superficie de la bacteria. Por su parte la gran movilidad de esta bacteria está dada por los flagelos: H. pylori posee entre dos y seis flagelos. Cada flagelo está compuesto por dos flagelinas, FlaA y FlaB. FlaB se localiza en la base del flagelo, y FlaA, que es la más abundante, se encuentra en el exterior. Estos flagelos son fundamentales para colonizar la mucosa gástrica, contrarrestando el peristaltismo y penetrando la capa de mucina secretada por las células de la superficie de la mucosa para alcanzar la superficie epitelial y escapar del ácido que la rodea.
En cuanto al gen cagA, se asocia a un riesgo incrementado para cáncer gástrico. Este es una proteína que es inyectada al interior celular a través de un sistema de secreción tipo IV, en el interior celular es fosforada e induce cambios morfológicos y probablemente de proliferación celular lo que favorece el desarrollo de gastritis y cáncer gástrico3. Las cepas CagA se han clasificado en dos tipos: cepas CagA positivas (CagA+) y cepas CagA negativas (CagA-), esta clasificación se basa en la presencia o no del gen asociado a la citotoxina A (cagA), el cual es uno de los 32 genes que constituyen la isla de patogenicidad Cag-PAI. Se ha demostrado que la proteína CagA que es inyectada en las células epiteliales gástricas a través del sistema de secreción tipo IV (T4SS) se comporta como una bacteria oncoproteica, por lo tanto cabe resaltar que las cepas que poseen un Cag-PAI positivo confieren mayor riesgo de cáncer gástrico que aquellas que tiene cepas cag negativos4, Las cepas cagA positivas (CagA+) inducen la reorganización de la actina en la célula huésped y en las proteínas de las células adyacentes al sitio de adherencia, mientras que las cepas CagA negativas (CagA-) inducen cambios mínimos en la actina en el sitio de adherencia2.
Por otro lado, la toxina vacuolizante (vacA) es codificada por el gen vaca, el cual se encuentra en la mayoría de las cepas. Esta tiene como función inducir la vacuolización, así como múltiples actividades celulares, incluyendo la formación de canales en la membrana, liberación del citocromo C de la mitocondria, el cual induce apoptosis, además se une a los receptores de las células de la membrana iniciando una respuesta proinflamatoria5. Cabe resaltar que el gen vacA posee tres regiones polimórficas denominadas región señal s1 (subtipos s1a, s1b y s1c) y s2; región intermedia (i1 e i2) y región media (m1 y m2). Debido a las combinaciones alélicas de las regiones señal y media, se presenta una variación en la actividad vacuolizante de las diferentes cepas de H. pylori, es decir, los aislamientos que presentan las combinaciones s1m1 y s1m2 producen niveles altos y moderados de citotoxina, respectivamente, mientras que los aislamientos con la combinación s2m2 producen muy poca citotoxina o no la producen. Todas estas variaciones alélicas de vacA pueden desencadenar una acción más persistente de la bacteria y una mayor progresión clínica de la lesión gástrica como factor de riesgo para cáncer gástrico1, es decir que la presencia de estas variaciones son de mal pronóstico para los pacientes que presentan infección por H. pylori.
Cabe resaltar que esta bacteria tiene una amplia capacidad para sobrevivir o adaptarse a condiciones extremadamente ácidas del entorno gástrico, estableciendo una infección persistente y desregulación de las funciones del huésped, lo que conduce a la patogénesis gástrica y al cáncer6, siendo el ambiente ácido uno los mecanismos de defensa de nuestro organismo contra las bacterias que son ingeridas con los alimentos7, por lo tanto, H. pylori presenta factores de patogenicidad que le permiten adaptarse al medio, produciendo sustancias que neutralizan los ácidos y formando una especie de nube protectora a su alrededor7, dentro de la cual se presenta la ureasa, la adhesina y genes como el vacA y el cagA, de modo que estos le proporcionan un medio de sobrevivencia y ayudan a la colonización del epitelio del estómago e intestino, de manera que si no es controlada de forma adecuada puede conllevar a causas como la gastritis crónica, dando como cofactor la formación de ulceras y en peor instancia el cáncer gástrico8.
Es importante señalar de manera detallada la patogenia de la infección por el H. pylori, la cual incluye dos etapas9: la primera se caracteriza por el ingreso de la bacteria, esta evade la actividad bactericida penetrando la mucosa gástrica, gracias a su motilidad y a la ureasa que como se dijo anteriormente hidroliza la urea en dióxido de carbono y amonio brindando la supervivencia de la bacteria en un medio ácido y la adhesina que la ayuda a adherirse a las células epiteliales11. H. pylori expresa la citosina vacuolizante (vacA), la cual tiene dos funciones, la primera adherirse a la membrana del epitelio gástrico, para promover nutrición de la bacteria, y la segunda es inducir la liberación de citocromo C de la mitocondria dando inicio a la apoptosis10.
La segunda etapa se caracteriza por la entrada de H. pylori al organismo causando una respuesta inespecífica que cumple un papel como respuesta inflamatoria, la cual está dada por el reclutamiento de células inflamatorias como macrófagos, neutrófilos y linfocitos, de manera que hacen parte de la defensa del huésped9. También proporciona el reconocimiento de agentes extraños, el cual se lleva a cabo por los macrófagos; estos se encargan de liberar citosinas como IL-6, induciendo una inflamación crónica y aumento de la producción de TNF-A como una sustancia proinflamatoria, IL-8, que se encarga de aumentar la permeabilidad celular y el reclutamiento y activación de los neutrófilos y la IL-10, la cual inhibe los linfocitos Th1, brindando una respuesta específica11. Esta etapa es muy importante debido a que se da la participación del sistema inmune local y sistémico en el control de la infección, y la neutralización de las toxinas bacterianas. Asimismo aumenta la destrucción tisular, ya sea según su intensidad y duración, la cual puede conducir a lesiones severas9.
Diversos estudios han mostrado una variabilidad de cepas de H. pylori, que explica la aparición de los síntomas, dentro de los cuales se presentan dolor, quemazón en la parte superior del abdomen, sensación de hinchazón del estómago, náuseas, vómitos, heces oscuras, anemia y saciedad rápida del hambre, por lo general, después de comer7.
Epidemiología de H. pylori y su
relación con el desarrollo
de otras enfermedades
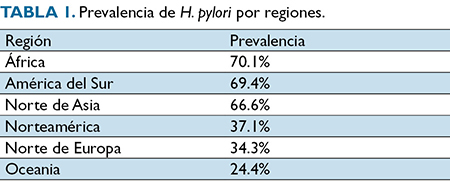
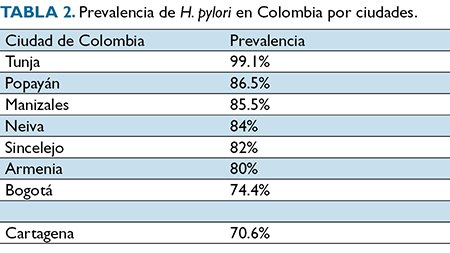
Actualmente la presencia de la H. pylori es considerada omnipresente en diferentes países, principalmente en el lejano Oriente. Su prevalencia está relacionada con un bajo índice socioeconómico y malas condiciones higiénicas. De acuerdo con un estudio de prevalencia se reportó una cifra de 48,5% a nivel mundial, con un rango de 70,1-24,4%12,13 (Tabla 1). Para países de Latinoamérica como Colombia, la prevalencia general de H. pylories 69,1% en las biopsias de estómago; sin embargo, los estudios son escasos14 (Tabla 2).
Este patógeno es considerado la principal causa de gastritis crónica, el principal agente etiológico de cáncer gástrico y la enfermedad ulceropéptica y, por último, también se ha relacionado con el linfoma del tejido linfoide asociado a las mucosas (MALT, por sus siglas en inglés: mucosa-associated lymphoid tissue)15,16. Actualmente existen estudios que relacionan la H. pylori con otras enfermedades como la enfermedad hepática grasa no alcohólica (NAFLD, por sus siglas en inglés: non alcoholic fat liver disease). Un estudio llevado a cabo para evaluar la asociación entre la infección por H. pylori y el riesgo de NAFLD mostró que la infección por H. pylori se asoció con un riesgo de 1,20 de NAFLD prevalente. Estos valores de riesgo se mantuvieron incluso después de corregir factores de confusión. También se mostró que la infección por H. pylori estaba asociada con aumento de la incidencia de NAFLD de 1,1417.
Estudios recientes han determinado que la H. pylori interfiere con procesos biológicos que influyen en la aparición de muchas enfermedades fuera del estómago y el duodeno, también se ha determinado un papel de H. pylori en la púrpura trombocitopénica idiopática y la anemia por deficiencia de hierro. La evidencia emergente sugiere que además puede contribuir a la deficiencia de vitamina B12, resistencia a la insulina, síndrome metabólico y diabetes mellitus, incluso puede aumentar el riesgo de síndrome coronario agudo, enfermedad cerebrovascular, enfermedad neurodegenerativa y otros trastornos. Se han formulado diversas hipótesis sobre mecanismos patógenos, incluida la aparición de mimetismo molecular y la inducción de una inflamación de bajo grado persistente que podría dar lugar a la presencia de estas patologías, lo que hace evidente la necesidad de una terapia de erradicación eficaz para combatir los efectos de la infección por H. Pylori15.
Métodos diagnósticos
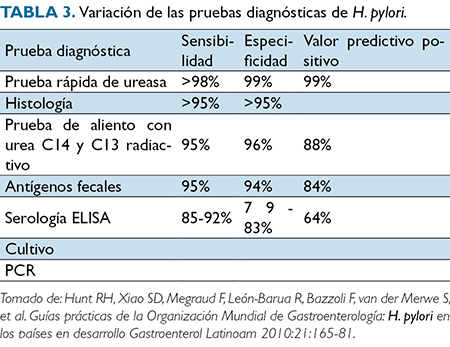
El diagnóstico actual incluye métodos endoscópicos y no endoscópicos o también llamados invasivos y no invasivos. Las técnicas utilizadas pueden ser directas (cultivo, demostración microscópica del microorganismo) o indirectas (utilizando ureasa, antígenos fecales, o una respuesta de anticuerpos como marcador de enfermedad). La elección del examen dependerá en su gran mayoría de la disponibilidad y el costo de estos, y además se debe tener en cuenta si estos exámenes son para evaluar si existe la infección o si ya ha sido erradicada la bacteria. Las pruebas con endoscopía incluyen la prueba rápida de ureasa (PRU), histología, cultivo, hibridación in situ por fluorescencia (FISH) y reacción en cadena de la polimerasa (PCR), y entre los exámenes sin endoscopía encontramos la prueba de antígenos fecales (SAT por su sigla en inglés), la prueba serológica por digitopunción, serología de sangre total, test de aliento con urea marcada con C13, test de aliento con urea marcada con C1418 (Tabla 3).
La prueba de ureasa se caracteriza por ser una prueba cualitativa en la que se busca valorar la actividad de la enzima ureasa, la cual indica de la presencia del microorganismo. Se realiza colocando una muestra de biopsia en un tubo de ensayo con urea que además contiene un indicador de cambio de pH. Lo que se espera es que si el microorganismo está presente la ureasa descomponga la urea en dióxido de carbono y amoníaco, lo cual aumenta el pH de la muestra y produce un cambio del color. Por su sencillez y rapidez puede ser usada para el diagnóstico inicial en aquellos pacientes que se someten a una endoscopia; sin embargo, dicha prueba suele perder sensibilidad cuando el paciente ha recibido tratamiento previo19,20.
Por su parte, la histología también es un método sencillo para determinar presencia de la H. pylori, específicamente la densidad de su colonización. Suelen utilizarse diferentes tinciones, entre ellas, hematoxilina-eosina, la de Warthin-Starry con nitrato de plata y la tinción con azul de metileno, actualmente sustituida por Giemsa por su bajo costo. Esta prueba es considerada como el estándar de oro para la detección de H. pylori debido a la observación directa de los cambios patológicos producidos por este patógeno. Debido a la migración y adaptación a cambios bioquímicos que puede tener la bacteria alrededor de la mucosa gástrica se recomienda la obtención de 3 biopsias en dos localizaciones diferentes, las cuales deben incluir el cuerpo y el antro; también es importante retirar los IBP (inhibidores de la bomba de protones) dos semanas antes de realizar el procedimiento18,19.
Existen técnicas complementarias como la histoquímica y la técnica de FISH que se han empleado para la detección de este patógeno; sin embargo es necesario un microscopio de fluorescencia, oligonucleótidos fluorescentes específicos y varios reactivos para su realización, por lo que suele ser poco utilizada debido a su alto costo19.
El cultivo suele ser altamente especifico y resulta útil para la clasificación genotípica de la H. pylori, diagnóstico microbiológico y determinación de sensibilidad y resistencia a antibióticos. Este microorganismo requiere una atmosfera microaerofílica, alta humedad, concentraciones de dióxido de carbono al 10% y temperaturas entre 36-37°C con un período de incubación de 3-14 días. Esta técnica es ideal para aquellos pacientes que presentan fallas en el tratamiento inicial ya que nos permite observar la sensibilidad del microorganismo y hacer un reajuste en el tratamiento. Sin embargo, se debe mencionar que, debido a la distribución heterogénea o también llamada en “parches” de H. pylori, resulta difícil la obtención de una muestra ideal, que sumado a los exigentes requerimientos de la bacteria para su crecimiento constituyen su principal desventaja19,20.
La reacción en cadena de la polimerasa permite la detección del ADN de la bacteria en la cual se logra la secuenciación de diferentes genes a través de unos cebadores. De todos los genes amplificados, el que se usa para el diagnóstico es el glmM, el cual ha permitido reportar una alta sensibilidad y especificidad con su uso. La PCR suele ser tan efectiva como el cultivo para confirmar la erradicación de la bacteria y determinar las fallas terapéuticas, además es muy útil con diferentes tipos de muestras. Una de sus desventajas la conforman los restos de las muestras de mucosa gástrica, lípidos y componentes que pueden originar falsos negativos19.
Las técnicas invasivas mencionadas anteriormente permiten estimar el compromiso del tejido gástrico y determinar la presencia de H. pylori, mientras que las técnicas no invasivas son útiles en la detección de infección activa. Entre las técnicas no invasivas encontramos a las pruebas serológicas que nos permiten la detección de anticuerpos IgG o IgA contra antígenos específicos de este patógeno. La IgG suele estar presente incluso 21 días después de adquirir la infección, lo cual revela infección activa o previa, constituyéndose como su principal desventaja. Los métodos más usados son: ensayo inmunoenzimático de enzima ligada (ELISA), aglutinación en látex, immunoblotting e inmunocromatografías (ICM), entre otras19,20.
La detección de antígenos fecales es otra técnica no invasiva que suele utilizarse cuando el test de aliento no está disponible, técnica que suele ser muy útil en niños por presentar mayor seguridad y menores costos. Actualmente hay dos pruebas disponibles en el mercado: la ELISA y el Ensayo Rápido inmunocromatográfico (ICT) utilizando anticuerpos policlonales o anticuerpos monoclonales. Las pruebas basadas en anticuerpos monoclonales muestran mejores resultados en comparación con las pruebas basadas en policlonales principalmente debido a la dificultad de obtener anticuerpos policlonales de calidad constante en todo momento. Las muestras de heces deben refrigerarse cuando se almacenan antes del análisis; de lo contrario, la sensibilidad de esta prueba se reducirá considerablemente. La precisión de esta prueba puede verse afectada por algunos problemas gastrointestinales, IBP, antibióticos y tratamientos con N-acetilcisteína (NAC) y úlceras sangrantes. Al igual que en la prueba de aliento con urea, los resultados falsos negativos se producen cuando la carga bacteriana es relativamente baja y debido al uso de antibióticos, bismuto e inhibidores de la bomba de protones20.
La prueba de aliento es considerada el gold standard de los métodos no invasivos para la detección de H. pylori. Esta prueba detecta la infección indirectamente midiendo la actividad de la ureasa bacteriana producida por H. pylori en el estómago. Se ingiere una suspensión de urea marcada con C13 o C14, se prefiere una urea marcada con C13 sobre C14 puesto que el C13 es estable y no radiactivo. La urea marcada se hidroliza en amoníaco y dióxido de carbono, que se difunde directamente en la sangre y se excreta a través de los pulmones y es exhalado a través del aliento, la cantidad de CO2 se mide para conocer la intensidad de hidrólisis de la urea, que estaría en relación con la presencia de ureasa y, por consiguiente, el microorganismo. Esta técnica es muy sensible y específica y, a diferencia de la prueba de ureasa, estudia toda la superficie del estómago. Sin embargo, resulta costosa y requiere de mucha habilidad, siendo esta su única desventaja21.
La utilización de una prueba u otra dependerá del contexto clínico. Cabe destacar que cada prueba tiene un propósito distinto: algunas son usadas para el diagnóstico de la infección antes del tratamiento y otras para confirmar su erradicación. De acuerdo con un estudio comparativo entre la prueba de antígenos fecales y el test de aliento con la histología (considerada el gold standard) se mostró una sensibilidad (S) y especificidad (E) de las pruebas en pretratamiento: Antígenos fecales S: 98%, E: 95%; pruebas del aliento, S y E de 100%; y en postratamiento ambas pruebas tuvieron S y E de 100%. Sin embargo, argumentan algunos sesgos en las publicaciones revisadas que pueden estar asociados según el estudio a un tamaño reducido o la calidad metodológica, concluyendo que la histología resulta ser el método más efectivo para el diagnóstico pretratamiento pero en el postratamiento son muy útiles las pruebas no invasivas como los antígenos fecales y el test de aliento22.
Estas dos últimas técnicas también han sido estudiadas en análisis comparativos para observar su eficacia en el postratamiento, concluyendo una menor especificidad por parte de la prueba de antígenos fecales, como muestra un estudio llevado a cabo por Bilardi et al., en donde luego de pruebas basadas en biopsias, la infección por H. pylori se erradicó en 77 pacientes pero continuó en 23, donde se observaron tres falsos negativos con HpSA (prueba de antígenos fecales) y dos con 13C-UBT (test de aliento con urea). Además, el número de falsos positivos fue significativamente mayor con HpSA que con 13C-UBT (nueve frente a uno)23.
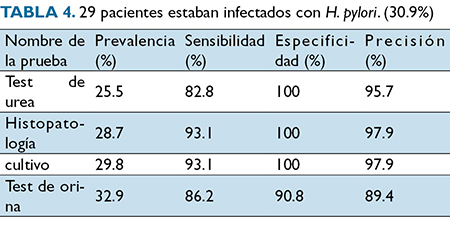
Actualmente han surgido nuevas técnicas para intentar realizar el diagnóstico de una manera más rápida, buscando métodos con una mayor sensibilidad, pero menos invasivos. Entre estos, la prueba de orina o RAPIRUN (por sus siglas en inglés), que fue inventada por Otsuka Pharmaceutical Co. Ltd. (Tokio, Japón) utilizando un ensayo inmunocromatográfico para la detección cualitativa de anticuerpos contra H. pylori en orina, fue aprobada por la FDA en 2006 y es usada en muchos países. Un estudio realizado para evaluar la eficacia de esta prueba en una población tailandesa mostró una alta sensibilidad y especificidad para dicha prueba, pero no superior a la de la histopatología, el cultivo y la prueba de ureasa24 (Tabla 4).
Pautas terapéuticas
En cuanto al tratamiento, es posible decir que se ha avanzado en la investigación de nuevos fármacos eficaces contra la erradicación de la H. pylori, aunque actualmente la resistencia sigue incrementando. Originalmente la terapia contra este patógeno incluye los inhibidores de la bomba de protones(IBP), amoxicilina y claritromicina, durante 7-14 días, pero debido a la creciente resistencia a la claritromicina también se ha venido sustituyendo con fármacos como el metronidazol y levofloxacino, que, sin embargo, también han reportado resistencia25. En algunos países la resistencia a la claritromicina puede llegar incluso al 80%26. Las guías actuales recomiendan el uso de esta en casos de que la resistencia sea inferior al 15% y, en el caso del metronidazol, menor de 40%, cuando sea necesario iniciar terapia empírica27.
En nuestro país la resistencia a la claritromicina, el metronidazol y levofloxacina es alta, de 13,6, 88 y 27,3 %, respectivamente28-30. Ello se debe al consumo generalizado de estos antibióticos y al inicio de terapias de manera empírica, porque no todos los centros cuentan con esta herramienta, lo cual puede conducir al fracaso terapéutico. Esto se evidencia a través de un estudio llevado a cabo en la ciudad de Bogotá, donde se muestra una multirresistencia a H. pylori en pacientes que fueron tratados previamente de manera empírica resultando en fracasos, donde ocho de los aislamientos presentaron resistencia a dos o más antibióticos, entre ellos amoxicilina, claritromicina y metronidazol, y además todos fueron resistentes a la levofloxacina. Por lo tanto, se ha venido recomendando utilizar las pruebas de susceptibilidad en los centros que cuenten con su disponibilidad para realizar la terapia inicial en todos los pacientes sin previo tratamiento31.
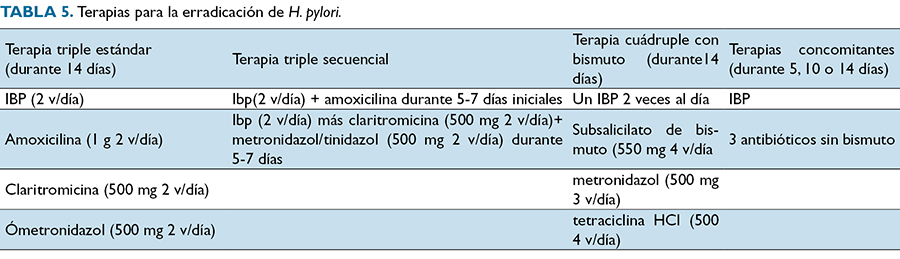
Actualmente en Colombia se sugiere utilizar la terapia triple secuencial o la triple estándar como primera línea teniendo en cuenta la resistencia antibióticos local y la terapia con mayor eficacia demostrada en la zona, esto debido a que los estudios han demostrado que el uso de terapia secuencial ha sido más eficaz (84,1 vs. 75,1) al erradicar la bacteria que la terapia triple estándar. Además, en aquellas zonas donde exista resistencia a los antibióticos claritromicina y metronidazol, se recomienda empezar con las terapias cuádruples con bismuto o terapias concomitantes27 (Tabla 5).
Recientemente se ha creado una cápsula denominada Pylera, comercializada principalmente en Europa, que contiene (bismuto, metronidazol y tetraciclina) para la terapia cuádruple con bismuto, con el fin de unificar el tiempo de toma de los antibióticos y reducir el volumen de fármacos, la cual ha tenido una eficacia en las cepas resistentes a metronidazol del 80-90% y también ha mostrado una ventaja estadísticamente significativa frente a la terapia triple estándar, por lo tanto se puede considerar como una terapia de primera línea eficaz en aquellos casos de resistencia al metronidazol13. Además, sus efectos adversos son escasos, un estudio que buscaba evaluar los efectos adversos en pacientes tratados con Pylera y un IBP mostró que solo 28,5% (57/200) de los pacientes experimentó efectos adversos y de estos solo a 7 sujetos los llevó a abandonar el tratamiento. Además, la efectividad basada en la intención de tratar fue de 91,5% y por protocolo fue de 95,2%32.
Es importante resaltar que para la selección de antibióticos se requieren los antecedentes farmacológicos de los pacientes, ya que las bacterias suelen hacer resistencias secundarias a fármacos como es el caso de la claritromicina y levofloxacino, a diferencia de lo que ocurre con el bismuto, la amoxicilina y la tetraciclina donde se reportan resistencias secundarias menores a 5%. En consecuencia, se debe interrogar al paciente por consumo previo de macrólidos en el caso de faringo amigdalitis o infecciones respiratorias previas, el uso de nitroimidazoles en el caso de las gastroenteritis o quinolonas para infecciones del tracto urinario o vías respiratorias, y por último indagar por el uso previo de tratamiento erradicador contra H. pylori. Es importante resaltar que nunca se debe repetir claritromicina o levofloxacino, en el caso de haberlo usado antes25.
Para las terapias de segunda línea se recomienda seguir con dos antibióticos diferentes a los usados en la terapia inicial. También se recomienda la terapia triple con moxifloxacino, levofloxacino o cuádruple con bismuto en aquellos casos en que no hayan sido utilizados como primera línea. Esto debido a una revisión de Zhang et al. donde se encontró diferencias en la seguridad y efectividad de las terapias de segunda línea con moxifloxacino en comparación con las terapias cuádruples con o sin bismuto (73,3% vs. 60,2%)27,33.
Por último, en cuanto a la supresión gástrica se ha recomendado el uso de fármacos inhibidores de la bomba de protones con una potente supresión del ácido gástrico debido a que a medida que aumenta el pH a 6-7 y se alcaliniza el medio gástrico, la H. pylori comienza su estado replicativo, pero con mayor susceptibilidad a antibióticos como la amoxicilina y la claritromicina24. Los IBP más usados frecuentemente son omeprazol, lansoprazol, pantoprazol, rabeprazol y esomeprazol. Recientemente ha surgido un nuevo fármaco inhibidor competitivo de los canales de potasio llamado vonoprazán, solamente disponible en Corea y Japón, que alcanza una supresión inmediata potente y sostenida, desarrollado por Takeda24. Un metaanálisis reciente encontró que las terapias con vonoprazán son más eficaces que las que utilizan los IBP convencionales, donde la tasa bruta de erradicación de H. pylori determinada por análisis de intención de tratar fue de 87,9% y 72,8% en la terapia triple basada en vonoprazán y la terapia triple basada en IBP, respectivamente34.
Los datos publicados sobre la eficacia y seguridad del vonoprazán en el tratamiento de la infección por H. pylori son todavía limitados. Un régimen de erradicación de 20 mg de vonoprazán + 750 mg de amoxicilina + 200 o 400 mg de claritromicina, dos veces al día durante 7 días, ha sido aprobado y está cubierto por el seguro de salud para tratamiento de primera línea en Japón desde 201535. En un estudio clínico de fase III, Murakami et al. observaron una tasa de erradicación de H. pylori de 92,6% con vonoprazán contra una tasa de 75,9% con lansoprazol, como parte de la terapia de primera línea36, además en los tratamientos de segunda línea la triple terapia con 250 mg de metronidazol + 750 mg de amoxicilina + 20 mg de vonoprazán, dos veces al día durante 7 días (aprobado y cubierto por el seguro de salud en Japón como terapia de segunda línea), resultó en una tasa de erradicación del 98%, posicionándose como uno de los fármacos más prometedores para la supresión gástrica del mercado37.
-
Uribe Echeverry PT, Acosta Cerquera MA, Arturo Arias BL, Jaramillo Arredondo MDS, BetancurPérez JF, Pérez Agudelo JM. Prevalencia genotípica de cagA y vacA en aislamientos de Helicobacter pylori de pacientes colombianos. Revista Cubana de Medicina Tropical 2018;70:18-26.
-
Martínez L, Márquez Y, Rodríguez BL, Reyes O, Mora S. Presencia del gen cagA y de la citotoxina vacA del Helicobacter pylori en pacientes dispépticos. Revista Cubana de Medicina Militar 2016;45:1–9.
-
González Vázquez R, Córdova Espinoza MG, Escamilla Gutiérrez A, Morales Méndez I, Ochoa Pérez SA, Armendáriz Toledano F, et al. Frecuencia de genes de virulencia en infecciones mixtas con cepas de Helicobacter pylori de una población mexicana. Revista de Gastroenterología de México 2016;81:11–20.
-
Yong X, Tang B, Li BS, Xie R, Hu CJ, Luo Get al. Helicobacter pylori virulence factor CagA promotes tumorigenesis of gastric cancer via multiple signaling pathways. Cell Commun Signal 2015;13:1–13.
-
Cervantes-García E. Helicobacter pylori: mecanismos de patogenicidad. Revista Latinoamericana de Patología Clínica y Medicina de Laboratorio 2016;63:100–9.
-
Camilo V, Sugiyama T, Touati E. Pathogenesis of Helicobacter pylori infection. Helicobacter 2017;22:1–6.
-
Fischbach W, Malfertheiner P. Helicobacter pylori infection. Deutsch Arzteblatt International 2018;115:429-36.
-
Bagheri N, Shirzad H, Elahi S, Azadegan Dehkordi F, Rahimian G, Shafigh M, et al. Downregulated regulatory T cell function is associated with increased peptic ulcer in Helicobacter pylori-infection. Microbial Pathogenesis 2017;110:165–75.
-
González Sosa G, Piñol Jiménez F. Etiopatogenia de la hemorragia digestiva alta no variceal, respuesta inflamatoria y Helicobacter pylori. Revista Médica Electrónica 2018;40:159–71.
-
Liu W, Zeng Z, Luo S, Hu C, Xu N, Huang A, et al. Gastric subserous vaccination with helicobacter pylori vaccine: An attempt to establish tissue-resident CD4+ memory T cells and induce prolonged protection. Frontiers in Immunology 2019;10:1–15.
-
Schmaußer B, Andrulis M, Endrich S, Lee SK, Josenhans C, Müller-Hermelink HK, et al. Expression and subcellular distribution of toll-like receptors TLR4, TLR5 and TLR9 on the gastric epithelium in Helicobacter pylori infection. Clinical and Experimental Immunology 2004;136:521–6.
-
Hooi JKY, Lai WY, Ng WK, Suen MMY, Underwood FE, Tanyingoh D, et al. Global Prevalence of Helicobacter pylori Infection: Systematic Review and Meta-Analysis. Gastroenterology 2017;153:420-9.
-
Leja M, Grinberga I, Bilgilier C, Steininger C. Review: Epidemiology of Helicobacter pylori infection. Helicobacter 2019;24:1-5
-
Bravo LE, Jaramillo R, Bravo PA. Helicobacter pylori: patología y prevalencia en biopsias gástricas en Colombia. Colombia Médica 2003;34:124-31.
-
Tsay FW, Hsu PI. H. pylori infection and extra-gastroduodenal diseases. Journal of Biomedical Science 2018;25:65.
-
Marshall BJ, Warren JR. Unidentified curved bacilli on gastric epithelium inactive chronic gastritis. Lancet 1984;I:1311-5.
-
Mantovani A, Turino T, Altomari A, Lonardo A, Zoppini G, Valenti L, et al. Association between Helicobacter pylori infection and risk of nonalcoholic fatty liver disease: An updated meta-analysis. Metabolism 2019;96:56-65.
-
Hunt RH, Xiao SD, Megraud F, León-Barua R, Bazzoli F, van der Merwe S, et al. Guías prácticas de la Organización Mundial de Gastroenterología: Helicobacter pylori en los países en desarrollo. Gastroenterología latinoamericana 2010; 21: 165-81.
-
Bermudez Díaz L, Torres Domínguez LE, Luis B, Rodriguez González BR. Métodos para la detección de la infección por Helicobacter pylori. Revista Cubana de Medicina 2008; 48: 1-14.
-
Frías Ordoñez JS, Otero Regino W. Aspectos prácticos en métodos diagnósticos para la infección por Helicobacter pylori: una revisión narrativa. Revista de Gastroenterología de Perú 2017;37:246-53.
-
Sabbagh P, Mohammadnia-Afrouzi M, Javanian M, Babazadeh A, Koppolu V, Vasigala VR, et al. Diagnostic methods for Helicobacter pylori infection: ideals, options, and limitations. European Journal of Clinical Microbiology and Infectious Diseases 2019;38:55-66.
-
Poveda YC, Reyes MM, Trespalacios AA, Otero W. Comparación de la prueba de antígenos fecales (Elisa) y test de aliento de la urea frente a histología para el diagnóstico de Helicobacter pylori: Revisión sistemática de la literatura.Revista Colombiana de Gastroenterología 2009;24:373-81.
-
Bilardi C, Biagini R, Dulbecco P, Iiritano E, Gambaro C, Mele MR, et al. Stool antigen assay (HpSA) is less reliable than urea breath test for post-treatment diagnosis of Helicobacter pylori infection. Alimentary Pharmacology and Therapeutics 2002;16:1733-8.
-
Aumpan N, Vilaichone R-K, Chotivitayatarakorn P, Pornthisarn B, Chonprasertsuk S, Bhanthumkomol P, et al. High Efficacy of Rapid Urine Test for Diagnosis of Helicobacter pylori Infection in Thai People. Asian Pacific Journal of Cancer Prevention 2019;20:1525-9.
-
Molina-Infante J, Corti R, Doweck J, McNicholl AG, Gisbert JP. Avances recientes en el tratamiento de la infección por Helicobacter pylori .Acta gastroenterológica latinoamericana 2017:75-85.
-
Escobedo-Belloc M, Bosques-Padilla F. El incremento en la resistencia al antibiótico de Helicobacter pylori en México: ¿son la azitromicina más levofloxacina la respuesta? Revista de Gastroenterología de México 2019;84: 271-73.
-
Otero W, Trespalacios AA,Otero L, Vallejo MT, Torres M, Pardo R, Sabbagh L. Guía de práctica clínica para el diagnóstico y tratamiento de la infección por Helicobacter pylori en adultos. Revista Colombiana de Gastroenterología 2015;30:17-33.
-
Atehortúa-Rendón JD, Martínez A, Pérez-Cala TL Descripción de la resistencia de Helicobacter pylori a seis antibióticos de uso frecuente en Colombia.Revista colombiana de Gastroenterología 2020;35:351-361.
-
Trespalacios AA, Otero Regino W, Mercado Reyes M. Helicobacter pylori resistance to metronidazole, clarithromycin and amoxicillin in Colombian patients. Revista Colombiana de Gastroenterología 2010;25:31-8.
-
Trespalacios AA, Otero W, Arévalo GA, Poutou RA, Rimbara E, Graham DY. Surveillance of levofloxacin resistance in Helicobacter pylori isolates in Bogotá-Colombia (2009-2014). PLoS ONE 2016;11:1-10.
-
Arévalo GA, Otero W, Trespalacios AA. Helicobacter pylori: resistencia múltiple en pacientes de Bogotá, Colombia. Biomédica 2019;39:125-3.
-
Castro Fernández M, Romero García T, Keco Huerga A, Pabón Jaén M, Lamas Rojas E, Llorca Fernández R, et al. Compliance, adverse effects and effectiveness of first line bismuth-containing quadruple treatment (Pylera) to eradicate Helicobacter pylori infection in 200 patients. Revista Española de Gastroenterología 2019;111:467-70.
-
Kim SG, Jung HK, Lee HL, et al. Guidelines for the diagnosis and treatment of Helicobacter pylori infection in Korea, 2013 revised edition. Journal of Gastroenterology andHepatology 2014;29:1371-86.
-
Jung YS, Kim EH, Park CH. Systematic review with meta-analysis: the efficacy of vonoprazan-based triple therapy on Helicobacter pylori eradication. Alimentary Pharmacology and Therapeutics 2017;46:106-14.
-
Akazawa Y, Fukuda D, Fukuda Y. Vonoprazan-based therapy for Helicobacter pylori eradication: experience and clinical evidence. Therapeutic Advances in Gastroenterology 2016;9:845-52.
-
Murakami K, Sakurai Y, Shiino M, Funao N, Nishimura A, Asaka M. Vonoprazan, a novel potassium-competitive acid blocker, as a component of first-line and second-line triple therapy for Helicobacter pylori eradication: a phase III, randomised, double-blind study. Gut 2016 ,65: 1439–1446.
-
O’Connor A, Furuta T, Gisbert JP, O’Morain C. Review – Treatment of Helicobacter pylori infection 2020. Helicobacter 2020;25:1-9.
María Nordmann-Ricardo
Programa de Medicina, Corporación Universitaria Rafael Núñez. Cartagena, Colombia..
Yiser Martínez1
Programa de Medicina, Corporación Universitaria Rafael Núñez. Cartagena, Colombia..
Daniela García1
Programa de Medicina, Corporación Universitaria Rafael Núñez. Cartagena, Colombia..
Odalys Cardona1
Programa de Medicina, Corporación Universitaria Rafael Núñez. Cartagena, Colombia..
Andrés Sánchez2
Grupo de investigación GINUMED, Programa de Medicina, Corporación Universitaria Rafael Núñez. Cartagena, Colombia. Clinical and Experimental Allergy Group (GACE), IPS University, University of Antioquia, Medellín, Colombia..
Marlon Múnera
Grupo de investigación GINUMED, Programa de Medicina, Corporación Universitaria Rafael Núñez. Cartagena, Colombia. Clinical and Experimental Allergy Group (GACE), IPS University, University of Antioquia, Medellín, Colombia..
Autor correspondencia
Marlon Múnera
Grupo de investigación GINUMED, Programa de Medicina, Corporación Universitaria Rafael Núñez. Cartagena, Colombia. Clinical and Experimental Allergy Group (GACE), IPS University, University of Antioquia, MedellÃn, Colombia..
Correo electrónico: marmunera@gmail.com.
Para descargar el PDF del artículo
Infección por Helicobacter pylori, una revisión actualizada
![]() Haga click aquí
Haga click aquí
Para descargar el PDF de la revista completa
Archivos de Alergia e Inmunología Clínica , Volumen Año 2021 Num 04
Archivos de Alergia e Inmunología Clínica
Número 04 | Volumen
52 | Año 2021
Editorial
Juan Carlos Muiño
Impacto de la dieta en la progresi�...
Diana Nossa y cols.
Infección por Helicobacter pylori,...
María Nordmann-Ricardo y cols.
Desarrollo de una APP para paciente...
Mariana Bonifacino Rodrigues y cols.
El valor de la determinación de se...
Silvana Haggi y cols.
Etiquetas
Helicobacter pylori, neoplasias gástricas, dispepsia, inhibidores de la bomba de protones
Tags
Helicobacter pylori, gastric neoplasms, dyspepsia, proton pump inhibitors
Infección por Helicobacter pylori, una revisión actualizada
Autores
María Nordmann-Ricardo, Yiser Martínez1, Daniela García1, Odalys Cardona1, Andrés Sánchez2, Marlon Múnera
Publicación
Archivos de Alergia e Inmunología Clínica
Editor
Asociación Argentina de Alergia e Inmunología Clínica
Fecha de publicación
2021-12-30
Registro de propiedad intelectual
© Asociación Argentina de Alergia e Inmunología Clínica